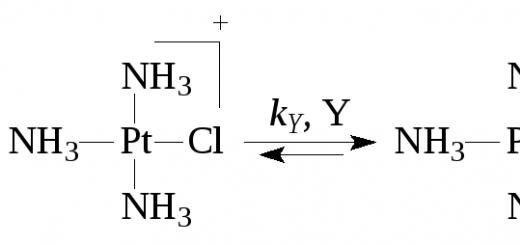
Гидролиз - это взаимодействие веществ с водой, в результате которого изменяется среда раствора.
Катионы и анионы слабых электролитов способны взаимодействовать с водой с образованием устойчивых малодиссоциируемых соединений или ионов, в результате чего меняется среда раствора. Формулы воды в уравнениях гидролиза обычно записывают в виде Н‑ОН. При реакции с водой катионы слабых оснований отнимают от воды гидроксил ион, и в растворе образуется избыток Н + . Среда раствора становится кислотной. Анионы слабых кислот притягивают из воды Н + , и реакция среды становится щелочной.
В неорганической химии чаще всего приходится иметь дело с гидролизом солей, т.е. с обменным взаимодействием ионов соли с молекулами воды в процессе их растворения. Различают 4 варианта гидролиза.
1. Соль образована сильным основанием и сильной кислотой.
Такая соль гидролизу практически не подвергается. При этом равновесие диссоциации воды в присутствии ионов соли почти не нарушается, поэтому рН=7, среда нейтральная.
Na + + H 2 O Cl ‑ + H 2 O
2. Если соль образована катионом сильного основания и анионом слабой кислоты, то происходит гидролиз по аниону.
Na 2 CO 3 + HOH \(\leftrightarrow\) NaHCO 3 + NaOH
Так как в растворе накапливаются ионы ОН ‑ , то среда - щелочная, рН>7.
3. Если соль образована катионом слабого основания и анионом сильной кислоты, то гидролиз идет по катиону.
Cu 2+ + HOH \(\leftrightarrow\) CuOH + + H +
СuCl 2 + HOH \(\leftrightarrow\) CuOHCl + HCl
Так как в растворе накапливаются ионы Н + , то среда кислая, рН<7.
4. Соль, образованная катионом слабого основания и анионом слабой кислоты, подвергается гидролизу и по катиону и по аниону.
CH 3 COONH 4 + HOH \(\leftrightarrow\) NH 4 OH + CH 3 COOH
CH 3 COO ‑ + + HOH \(\leftrightarrow\) NH 4 OH + CH 3 COOH
Растворы таких солей имеют или слабокислую, или слабощелочную среду, т.е. величина рН близка к 7. Реакция среды зависит от соотношения констант диссоциации кислоты и основания. Гидролиз солей, образованных очень слабыми кислотой и основанием, является практически необратимым. Это, в основном, сульфиды и карбонаты алюминия, хрома, железа.
Al 2 S 3 + 3HOH \(\leftrightarrow\) 2Al(OH) 3 + 3H 2 S
При определении среды раствора солей необходимо учитывать, что среда раствора определяется сильным компонентом. Если соль образована кислотой, являющейся сильным электролитом, то среда раствора кислая. Если основание сильный электролит, то - щелочная.
Пример. Щелочную среду имеет раствор
1) Pb(NO 3) 2 ; 2) Na 2 CO 3 ; 3) NaCl; 4) NaNO 3
1) Pb(NO 3) 2 нитрат свинца(II). Соль образована слабым основанием и сильной кислотой , значит среда раствора кислая.
2) Na 2 CO 3 карбонат натрия. Соль образована сильным основанием и слабой кислотой, значит среда раствора щелочная.
3) NaCl; 4) NaNO 3 Соли образованы сильным основанием NaOH и сильными кислотами HCl и HNO 3 . Среда раствора нейтральная.
Правильный ответ 2) Na 2 CO 3
В растворы солей опустили индикаторную бумажку. В растворах NaCl и NaNO 3 она не изменила цвет, значит среда раствора нейтральная . В растворе Pb(NO 3) 2 окрасилась в красный цвет, среда раствора кислая. В растворе Na 2 СO 3 окрасилась в синий цвет, среда раствора щелочная.
Методическая разработка урока
«Среда водных растворов»
Цель: формирование исследовательской компетенции обучающихся при изучении среды водных растворов электролитов и методов ее качественного анализа.
Задачи:
- Сформировать представление обучающихся о типах среды водных растворов (кислая, нейтральна, щелочная);
- Рассмотреть понятие «индикаторы» и основные виды индикаторов (лакмус, фенолфталеин, метиловый оранжевый);
- Изучить изменение окраски индикаторов в разных средах;
- Выявить в ходе химического эксперимента наиболее оптимальный индикатор для определения кислой и щелочной среды раствора;
- Проанализировать зависимость между средой раствора и значением водородного показателя;
- Сформировать навыки работы обучающихся с универсальным индикатором;
- Выявить зависимость окраски соков некоторых растений (в частности капусты краснокочанной) от среды раствора.
Форма: урок – исследование. Данная форма позволяет моделировать все этапы химического исследования при изучении конкретной темы.
На данном уроке гармонично сочетаются проблемный метод и химический эксперимент, служащий средством доказательства или опровержения выдвинутых гипотез.
Ведущая форма деятельности на уроке – самостоятельная работа обучающихся в парах или группах, выполняющих одинаковые или разные задания (по вариантам), направленные на получение более широкого круга информации всем классом.
Методические комментарии записаны курсивом.
Оргмомент. I этап - мотивационный
Добрый день! Мир, окружающий нас, полон разнообразных по строению и свойствам веществ. Познание их позволит нам познать самих себя.
Самым оптимальным и емким способом познания является исследование. Сегодня я предлагаю нам представить себя не учениками и учителем, а сотрудниками серьезной лаборатории, маститыми учеными-исследователями химии.(Игровые технологии) Слайд №1
Для начала позвольте мне задать Вам вопрос, который был адресован мне одним из моих коллег: «Что общего между древним Карфагеном и современной Голландией?» (проблемное обучение) (Обсуждение вариантов ответа)
На самом деле общими являются экологические проблемы, характерные и для одного, и для другого государства.
Историческая справка: В свое время Карфаген был очень мощным государством, которое отстаивало свое господство на Средиземноморье. В результате третьей Пунической войны полумиллионный город Карфаген был полностью уничтожен, а оставшиеся в живых жители проданы в рабство. Римляне скандировали: «Carthago delendam esse!» («Карфаген должен быть уничтожен!»). Слайд №2
Место, где располагался город, было засыпано солью. Современную Голландию никто солью не засыпает, но это государство активно борется с мировыми экологическими проблемами, в том числе вызываемыми наводнения. (межпредметные связи)
Проблемный вопрос:
Как вы думаете, в Егорьевске имеются экологические проблемы? Какие?
(Засорение почвы, загрязнение водоемов, атмосферы, много мусора на улицах и т.д.)
Одна из важнейших проблем – проблема чистоты воды . Вода поступает в водопровод с насосных станций, поднимающих её с большой глубины, из артезианских скважин. А ведь когда-то источником воды в селе Высоком (на месте которого возник Егорьевск) была река Гуслица.Слайд №3
Рассмотрим современный образец воды из реки Гуслица. Оцените цвет, прозрачность, запах, наличие взвешенных частиц.
Все эти методы анализа относятся к органолептическим. Объясните название понятия . (Т.е. осуществляются с помощью органов чувств человека).
Вопрос для размышления :Основываясь только на результатах органолептических методов, можно сделать вывод об экологической чистоте образцов воды?
(Нельзя. В воде могут содержаться частицы, которые мы не видим – внешне незаметные).
Мы подошли к проблеме : Как определить наличие невидимых частиц в растворе? (проблемное обучение)
II этап - Решение проблемы
Цель нашего сегодняшнего исследования: изучить некоторые способы качественного анализа водных растворов (т.е. содержания в них разных частиц). Какими способами можно воспользоваться?
(Можно проводить химические реакции – качественные реакции , доказывающие наличие в растворе тех или иных частиц.)
А можно воспользоваться специальными веществами – индикаторами .
Вопрос для размышления: Вы знакомы с индикаторами из курса биологии, физики и других учебных дисциплин. Как Вы думаете, какое значение в химии имеет термин «индикатор»?
Фиксация определения на слайде:Слайд № 4
Индикатор – это вещество, изменяющее свой цвет в зависимости от среды раствора.
Вопрос для размышления: Все ли Вам понятно в данном определении?
(Что такое «среда раствора»? Какая она бывает?) Это тема нашего сегодняшнего урока, запишите ее в тетради:
« Среда водных растворов ».
Выявить типы сред водных растворов Вам поможет великая наука – логика!... и знание классов неорганических соединений.
Предлагаю построить первую логическую цепочку, ответив на соответствующие вопросы:
- К какому классу относятся вещества с формулами: HCl, H 2 SO 4 , HNO 3 , H 2 S? (кислоты)Слайд №5
- Какие катионы образуются в растворе при диссоциации данного класса соединений? (катионы водорода)
Записать на доске уравнение диссоциации азотной кислоты
HNO 3 → H + + NO 3 -
Подсказка: Название среды раствора в данном случае происходит от названия соответствующего класса соединений (кислая среда ).
- Постройте следующую логическую цепочку для соединений, выраженных формулами: NaOH, Ca(OH) 2 , KOH, Ba(OH) 2 . (основания, щёлочи) Слайд №6
Записать на доске уравнение полной диссоциации гидроксида бария
Ba(OH) 2 → Ba 2+ + 2OH -
Подсказка: Вспомните классификацию оснований! Все ли основания в водном растворе распадаются на ионы? Название среды происходит от названия растворимых оснований. (щелочная)
- К какому классу относятся следующие вещества: сульфат калия, хлорид бария, нитрат кальция? (соли). Слайд №7 K 2 SO 4 , BaCl 2 , Ca(NO 3) 2
- При растворении в воде данных соединений образуются частицы, характеризующие кислотный или щелочной характер раствора? (не образуются)
Составить на доске уравнение диссоциации сульфата калия
K 2 SO 4 → 2K + + SO 4 2-
Подсказка: Название среды происходит от отсутствия катионов водорода и анионов гидроксо-групп. (нейтральная)
Составим схему классификации сред Схема на доске (педагогика сотрудничества)
СРЕДА ВОДНЫХ РАСТВОРОВ
_______________ ________________
___________________
(физкультминутка для глаз)
Итак, мы выяснили, что существуют три типа среды водных растворов (кислая, нейтральная и щелочная).
Измерить уровень кислотности водной среды нам помогут индикаторы, о которых мы уже говорили вначале урока.
Индикаторы – это вещества, изменяющие свой цвет в зависимости от среды раствора.
Индикаторы бывают разные. Сегодня мы с Вами познакомимся с тремя основными: синий лакмус, метиловый оранжевый и фенолфталеин .
Каждый из них по-разному изменяет окраску в зависимости от среды раствора, поэтому наша с Вами задача – подобрать наиболее оптимальный индикатор для каждой среды раствора.
Для работы сделаем таблицу:Слайд №9
|
Метилоранж |
Фенолфталеин |
||
|
Раствор кислоты |
|||
|
Раствор щёлочи |
|||
|
Раствор соли |
В три пробирки налейте по 2-3 мл раствора соляной кислоты. В каждую из них добавьте по 1 капле индикаторов (в пробирку № 1 – метиловый оранжевый, в пробирку № 2 - фенолфталеин, в пробирку № 3 – синий лакмус).
Зафиксируйте наблюдаемые изменения в тетради.
Задание: Отметьте название индикатора, который наиболее удобно использовать для определения кислой среды водного раствора!
В три пробирки налейте по 2-3 мл раствора гидроксида натрия. В каждую из них добавьте по 1 капле индикаторов (в пробирку № 1 – метиловый оранжевый, в пробирку № 2 - фенолфталеин, в пробирку № 3 – синий лакмус).
Пронаблюдайте за изменением окраски. Зафиксируйте наблюдаемые изменения в тетради
Задание: Отметьте название индикатора, который наиболее удобно использовать для определения щелочной среды водного раствора!
Обсуждение результатов эксперимента. Заполнение таблицы в тетради (обучающиеся) и на слайде (учителем). (педагогика сотрудничества)
Формулирование выводов: В кислой среде окраска метилового оранжевого становится красной, лакмуса – красной, фенолфталеин не изменяет своей окраски. Следовательно, наиболее оптимальный индикатор для определения кислой среды раствора – метиловый оранжевый .
В щелочной среде окраска метилового оранжевого становится желтой, лакмуса – синей, фенолфталеина – малиновой. Следовательно, наиболее оптимальный индикатор для определения щелочной среды - фенолфталеин.
Вы вооружились новыми знаниями. Можете вы теперь изучить среду образца воды?
Попробуйте определить средуобразца воды, используя оптимальные индикаторы, только для этого отлейте изхимического стаканчика небольшое количество исследуемой воды в три чистые пробирки и добавьте в каждую соответствующий индикатор (фенолфталеин, метиловый оранжевый).
Наблюдаете ли Вы значительные изменения окраски индикаторов в растворах? (Нет).
Какие гипотезы Вы можете выдвинуть?
- Среда раствора не сильно кислая, или не сильно щелочная, поэтому индикаторы не могут уловить разницу.
- Среда нейтральная, поэтому окраска индикаторов не изменяется.
Действительно, диапазон характеристики среды раствора очень широк: от сильнокислой до сильнощелочной.
Он выражается в единицах от 0 до 14, которые называются значением рН (пэ-аш) – водородным показателем .(опережающее обучение)
Водородный показатель – величина, характеризующая содержание катионов водорода в растворе. Есть точные универсальные индикаторы. Слайд №10
Опережающее обучение. С научной точки зрения рН – это отрицательный десятичный логарифм концентрации ионов водорода в растворе. Пока здесь для Вас очень много непонятных слов, но в 11 классе мы вернемся к изучению этой величины и будем рассматривать ее более подробно с позиции тех знаний, которые Вы к тому времени будете иметь.
Задание в тетради :
Используя полученные сведения, выявите взаимосвязь меду значением рН и средой раствора. Выводы оформите в тетради.
Выводы:
При рН > 7 среда раствора щелочная
При рН = 7 среда раствора нейтральная
При рН < 7 среда раствора кислая
Для определения значения рН и более точного определения среды раствора существуют разные методы: кислотно-основное титрование, измерением электродвижущей силы (ЭДС), а можно с помощью универсальной индикаторной бумаги.
В образец воды в химическом стаканчике опустите универсальную индикаторную бумагу.
Сравните полученную на ней окраску с цветной шкалой рН.
Вопрос для размышления : Какова среда раствора выданного Вам образца?
Обязательно стоит уточнить тип среды по силе (слабо-, сильно-).
Проблемный вопрос :Ну а теперь Вы можете сделать вывод об экологическом состоянии выданного вам образца воды?
(Нет. Потому что мы не знаем экологических норм, не знаем, с чем сравнить наши образцы).
Сравнить уровень кислотности выданных образцов Вы можете с условной шкалой значений рН некоторых растворов.
На слайде составляется шкала значений рН Слайд №11
Проблемные вопросы :
- Как Вы думаете, какие жидкости не рекомендуется употреблять людям с язвенной болезнью желудка? Почему?
(Все слабо- и сильно кислые растворы (кофе, лимонный, яблочный, томатный сок, Кока-кола) могут вызвать обострение язвенной болезни из-за излишней кислотности).
- Что общего, на Ваш взгляд, между нашатырным спиртом, который хозяйки добавляют в воду для мытья стекол, и мылом, которым мы с Вами моем руки?
(И раствор мыла, и нашатырный спирт имеют щелочную среду, которая способствует удалению грязи). Слайд №12
Проблемный вопрос :Иногда нам бывает необходимо определить среду раствора в домашних условиях. А под руками нет универсальной индикаторной бумаги. Что делать? (проблемное обучение)
Информация: Оказывается, некоторые овощи и фрукты обладают индикаторной способностью. Они содержат в себе рН-чувствительный пигмент (антоцианин).
Это плоды темно-синего, фиолетового цвета: свекла, ежевика, черная смородина, вишня, темный виноград и, в том числе краснокочанная капуста.
Информация : В домашних условиях Вы можете изготовить индикаторные бумажки.
Возьмите сок краснокочанной капусты и пропитайте им листки фильтровальной бумаги. Листкам надо дать высохнуть. После этого разрежьте фильтровальную бумагу на тонкие полоски. Индикаторные бумажки готовы! Успешных Вам экспериментов! (гуманно-личностное)
III этап. Заключительный этап исследования :
Мы с Вами подходим к концу нашего исследования. Ранее вы сказали, что для того, чтобы сделать вывод о соответствии норме кислотности образцов воды мы должны владеть полезной информацией о санитарно-гигиенических нормах, действующих в мире и в нашей стране.
Полезная информация :В соответствии с Гигиеническими требованиями к качеству воды централизованных систем питьевого водоснабжения (СанПиН 2.1.4.559-96) питьевая вода должна быть безвредна по химическому составу и иметь благоприятные органолептические свойства.
Водородный показатель для питьевой воды должен соответствовать норме 6-9 единиц, для водоемов 6,5 – 8,5.Исследователи установили, что особенно губительным для водных обитателей является кислая среда, нежели щелочная. У водных растений повышение кислотности воды, в первую очередь, сказывается на нарушении кальциевого обмена и образовании оболочек клеток, их делении, а также на протекании реакции фотосинтеза.
Для водных объектов и питьевой воды содержание нитратов не должно превышать 45 мг/л, фосфатов – 3,5 мг/л. Нитрат- и фосфат – ионы способствуют зарастанию водоемов растительностью, вызывая разрастание планктона. Тот, в свою очередь, отмирает и поглощает большое количество кислорода, лишая воду способности к самоочищению. Нитраты могут оказать токсическое действие на людей и водных обитателей.
Повышенное содержание железа в воде вызывает отложение железа в печени и по вредности значительно обгоняет алкоголизм. Предельно-допустимая концентрация в воде железа составляет 0,3 мг/л. (здоровьесберегающие технологии)
III. Рефлексия Вопросы для обсуждения :
- Соответствует ли норме значения рН исследуемой воды?
- В каких препаратах раствор имеет кислую среду?
- В каких препаратах среда раствора щелочная?
- Как изменяют окраску индикаторы в подобной среде?
Ключевой вопрос :
Как Вы полагаете, полученных на данный момент сведений о качестве образцов воды достаточно, чтобы сделать окончательный вывод о ее экологической пригодности и чистоте?(Не достаточно. Нужно провести полный качественный анализ на содержание в ней разных частиц – ионов).
Вывод: нужно долго и кропотливо изучать предмет, чтобы делать полные и правильные выводы из исследований.
Д.З. параграф 28, упр. №2,3 стр. 46
Для того, чтобы понять, что такое гидролиз солей, вспомним для начала, как диссоциируют кислоты и щелочи.
Общим между всеми кислотами является то, что при их диссоциации обязательно образуются катионы водорода (Н +), при диссоциации же всех щелочей всегда образуются гидроксид-ионы (ОН −).
В связи с этим, если в растворе, по тем или иным причинам, больше ионов Н + говорят, что раствор имеет кислую реакцию среды, если ОН − — щелочную реакцию среды.
Если с кислотами и щелочами все понятно, то какая же реакция среды будет в растворах солей?
На первый взгляд, она всегда должна быть нейтральной. И правда же, откуда, например, в растворе сульфида натрия взяться избытку катионов водорода или гидроксид-ионов. Сам сульфид натрия при диссоциации не образует ионов ни одного, ни другого типа:
Na 2 S = 2Na + + S 2-
Тем не менее, если бы перед вами оказались, к примеру, водные растворы сульфида натрия, хлорида натрия, нитрата цинка и электронный pH-метр (цифровой прибор для определения кислотности среды) вы бы обнаружили необычное явление. Прибор показал бы вам, что рН раствора сульфида натрия больше 7, т.е. в нем явный избыток гидроксид-ионов. Среда раствора хлорида натрия оказалась бы нейтральной (pH = 7), а раствора Zn(NO 3) 2 кислой.
Единственное, что соответствует нашим ожиданиям – это среда раствора хлорида натрия. Она оказалась нейтральной, как и предполагалось.
Но откуда же взялся избыток гидроксид-ионов в растворе сульфида натрия, и катионов-водорода в растворе нитрата цинка?
Попробуем разобраться. Для этого нам нужно усвоить следующие теоретические моменты.
Любую соль можно представить как продукт взаимодействия кислоты и основания. Кислоты и основания делятся на сильные и слабые. Напомним, что сильными называют те кислоты, и основания, степень диссоциации, которых близка к 100%.
примечание: сернистую (H 2 SO 3) и фосфорную (H 3 PO 4) чаще относят к кислотам средней силы, но при рассмотрении заданий по гидролизу нужно относить их к слабым.
Кислотные остатки слабых кислот, способны обратимо взаимодействовать с молекулами воды, отрывая от них катионы водорода H + . Например, сульфид-ион, являясь кислотным остатком слабой сероводородной кислоты, взаимодействует с ней следующим образом:
S 2- + H 2 O ↔ HS − + OH −
HS − + H 2 O ↔ H 2 S + OH −
Как можно видеть, в результате такого взаимодействия образуется избыток гидроксид-ионов, отвечающий за щелочную реакцию среды. То есть кислотные остатки слабых кислот увеличивают щелочность среды. В случае растворов солей содержащих такие кислотные остатки говорят, что для них наблюдается гидролиз по аниону .
Кислотные остатки сильных кислот, в отличие от слабых, с водой не взаимодействуют. То есть они не оказывают влияния на pH водного раствора. Например, хлорид-ион, являясь кислотным остатком сильной соляной кислоты, с водой не реагирует:
То есть, хлорид-ионы, не влияют на pН раствора.
Из катионов металлов, так же с водой способны взаимодействовать только те, которым соответствуют слабые основания. Например, катион Zn 2+ , которому соответствует слабое основание гидроксид цинка. В водных растворах солей цинка протекают процессы:
Zn 2+ + H 2 O ↔ Zn(OH) + + H +
Zn(OH) + + H 2 O ↔ Zn(OH) + + H +
Как можно видеть из уравнений выше, в результате взаимодействия катионов цинка с водой, в растворе накапливаются катионы водорода, повышающие кислотность среды, то есть понижающие pH. Если в состав соли, входят катионы, которым соответствуют слабые основания, в этом случае говорят что соль гидролизуется по катиону .
Катионы металлов, которым соответствуют сильные основания, с водой не взаимодействуют. Например, катиону Na + соответствует сильное основание – гидроксид натрия. Поэтому ионы натрия с водой не реагируют и никак не влияют на pH раствора.
Таким образом, исходя из вышесказанного соли можно разделить на 4 типа, а именно, образованные:
1) сильным основанием и сильной кислотой,
Такие соли не содержат ни кислотных остатков, ни катионов металлов, взаимодействующих с водой, т.е. способных повлиять на pH водного раствора. Растворы таких солей имеют нейтральную реакцию среды. Про такие соли говорят, что они не подвергаются гидролизу .
Примеры: Ba(NO 3) 2 , KCl, Li 2 SO 4 и т.д.
2) сильным основанием и слабой кислотой
В растворах таких солей, с водой реагируют только кислотные остатки. Среда водных растворов таких солей щелочная, в отношении солей такого типа говорят, что они гидролизуются по аниону
Примеры: NaF, K 2 CO 3 , Li 2 S и т.д.
3) слабым основанием и сильной кислотой
У таких солей с водой реагируют катионы, а кислотные остатки не реагируют – гидролиз соли по катиону , среда кислая.
Примеры: Zn(NO 3) 2 , Fe 2 (SO 4) 3 , CuSO 4 и т.д.
4) слабым основанием и слабой кислотой.
С водой реагируют как катионы, так и анионы кислотных остатков. Гидролиз солей такого рода идет и по катиону, и по аниону или же. Также говорят про такие соли, что они подвергаются необратимому гидролизу .
Что же значит то, что они необратимо гидролизуются?
Поскольку в данном случае с водой реагируют и катионы металла (или NH 4 +) и анионы кислотного остатка, в раcтворе одновременно возникают и ионы H + , и ионы OH − , которые образуют крайне малодиссоциирующее вещество – воду (H 2 O).
Это, в свою очередь, приводит к тому, что соли образованные кислотными остатками слабых оснований и слабых кислот не могут быть получены обменными реакциями, а только твердофазным синтезом, либо и вовсе не могут быть получены. Например, при смешении раствора нитрата алюминия с раствором сульфида натрия, вместо ожидаемой реакции:
2Al(NO 3) 3 + 3Na 2 S = Al 2 S 3 + 6NaNO 3 (− так реакция не протекает!)
Наблюдается следующая реакция:
2Al(NO 3) 3 + 3Na 2 S + 6H 2 O= 2Al(OH) 3 ↓+ 3H 2 S + 6NaNO 3
Тем не менее, сульфид алюминия без проблем может быть получен сплавлением порошка алюминия с серой:
2Al + 3S = Al 2 S 3
При внесении сульфида алюминия в воду, он также как и при попытке его получения в водном растворе, подвергается необратимому гидролизу.
Al 2 S 3 + 6H 2 O = 2Al(OH) 3 ↓ + 3H 2 S
Гидролиз - это обменная реакция вещества с водой, приводящая к его разложению . Попробуем разобраться в причине данного явления.
Электролиты делятся на сильные электролиты и слабые. См. Табл. 1.
Вода относится к слабым электролитам и поэтому диссоциирует на ионы лишь в незначительной степени Н2О ↔ Н++ ОН-
Ионы веществ, попадающие в раствор, гидратируются молекулами воды. Но при этом может происходить и другой процесс. Например, анионы соли, которые образуются при её диссоциации, могут взаимодействовать с катионами водорода, которые, пусть и в незначительной степени, но все-таки образуются при диссоциации воды. При этом может происходить смещение равновесия диссоциации воды. Обозначим анион кислоты Х-.
Предположим, что кислота сильная. Тогда она по определению практически полностью распадается на ионы. Если кислота слабая , то она диссоциирует неполностью. Она будет образовываться при прибавлении в воду из анионов соли и ионов водорода, получающихся при диссоциации воды. За счет её образования, в растворе будут связываться ионы водорода, и их концентрация будет уменьшаться. Н++ Х-↔ НХ
Но, по правилу Ле Шателье, при уменьшении концентрации ионов водорода равновесие смещается в первой реакции в сторону их образования, т. е. вправо. Ионы водорода будут связываться с ионами водорода воды, а гидроксид ионы - нет, и их станет больше, чем было в воде до прибавления соли. Значит, среда раствора будет щелочная . Индикатор фенолфталеин станет малиновым. См. рис. 1.
Аналогично можно рассмотреть взаимодействие катионов с водой. Не повторяя всю цепочку рассуждений, подытоживаем, что если основание слабое , то в растворе будут накапливаться ионы водорода, и среда будет кислая .
Катионы и анионы солей можно разделить на два типа. Рис. 2.
Рис. 2. Классификация катионов и анионов по силе электролитов
Поскольку и катионы и анионы, согласно данной классификации, бывают двух типов, то всего существует 4 разнообразных комбинации при образовании их солей. Рассмотрим, как относится к гидролизу каждый из классов этих солей. Табл. 2.
|
Какими по силе кислотой и основанием образована соль |
Примеры солей |
Отношение к гидролизу |
Среда |
Окраска лакмуса |
|
Соль сильного основания и сильной кислоты |
NaCl, Ba(NO3)2, K2SO4 |
Гидролизу не подвергаются. |
нейтральная |
фиолетовый |
|
Соль слабого основания и сильной кислоты |
ZnSO4, AlCl3, Fe(NO3)3 |
Гидролиз по катиону. Zn2+ + HOH ZnOH+ + H+ |
||
|
Соль сильного основания и слабой кислоты |
Na2CO3,К2SiO3, Li2SO3 |
Гидролиз по аниону CO32 + HOH |
щелочная |
|
|
Соль слабого основания и слабой кислоты |
FeS, Al(NO2)3, CuS |
Гидролиз и по аниону, и по катиону. |
среда раствора зависит от того, какое из образующихся соединений будет более слабым электролитом. |
зависит от более сильного электролита. |
Усилить гидролиз можно разбавлением раствора или нагреванием системы.
Соли, которые подвергаются необратимому гидролизу
Реакции ионного обмена протекают до конца при выпадении осадка, выделения газа или малодиссоируемого вещества.
2 Al (NO3)3+ 3 Na2S +6 Н 2 О → 2 Al (OH)3 ↓+ 3 H2S+6 NaNO3 (1)
Если взять соль слабого основания и слабой кислоты и при этом и катион, и анион будут многозарядным, то при гидролизе таких солей будет образовываться и нерастворимый гидроксид соответствующего металла, и газообразный продукт. В данном случае гидролиз может стать необратимым. Например, в реакции (1) не образуется осадок сульфида алюминия.
Под это правило подпадают следующие соли: Al2S3, Cr2S3, Al2(CO3)3, Cr2(CO3)3, Fe2(CO3)3, CuCO3. Эти соли в водной среде подвергаются необратимому гидролизу. Их невозможно получить в водном растворе.
В органической химии гидролиз имеет очень большое значение.
При гидролизе изменяется концентрация ионов водорода в растворе, а во многих реакциях используются кислоты или основания. Поэтому, если мы будем знать концентрацию ионов водорода в растворе, то будет легче следить за процессом и управлять им. Для количественной характеристики содержания ионов в растворе используется pН раствора. Он равен отрицательному логарифму концентрации ионов водорода.
p Н = - lg [ H + ]
Концентрация ионов водорода в воде равна 10-7 степени, соответственно, рН = 7 у абсолютно чистой воды при комнатной температуре.
Если долить в раствор кислоты или добавить соль слабого основания и сильной кислоты, то концентрация ионов водорода станет больше 10-7и рН < 7.
Если добавить щелочи или соли сильного основания и слабой кислоты, то концентрация ионов водорода станет меньше, чем 10-7и рН>7. См. рис. 3. Знать количественный показатель кислотности необходимо во многих случаях. Например, водородный показатель желудочного сока равен 1,7. Увеличение или уменьшение этого значения приводит к нарушению пищеварительных функций человека. В сельском хозяйстве ведется контроль кислотности почвы. Например, для садоводства наилучшей является почва с рН = 5-6. При отклонении от этих значений в почву вносят подкисляющие или подщелачивающие добавки.

ИСТОЧНИКИ
источник видео - http://www.youtube.com/watch?v=CZBpa_ENioM
источнки презентации - http://ppt4web.ru/khimija/gidroliz-solejj-urok-khimii-klass.html
Соли – это ионные соединения, при попадании в воду они диссоциируют на ионы. В водном растворе эти ионы ГИДРАТИРОВАНЫ – окружены молекулами воды.
Обнаружено, что водные растворы многих солей имеют не нейтральную среду, а либо слабокислую, либо щелочную.
Объяснение этого – взаимодействие ионов соли с водой. Этот процесс называется ГИДРОЛИЗОМ.
Катионы и анионы, образованные слабым основанием или слабой кислотой, взаимодействуют с водой, отрывая от нее Н или ОН.
Причина этого: образование БОЛЕЕ ПРОЧНОЙ связи, чем в самой воде.
По отношению к воде соли можно разделить на 4 группы:
1) Соль, образованная сильным основанием и сильной кислотой - НЕ ГИДРОЛИЗУЕТСЯ , в растворе только диссоциирует на ионы. Среда нейтральная. ПРИМЕР: Не гидролизуются соли – NaCl, KNO3, RbBr, Cs2SO4, KClO3, и т. п. В растворе эти соли только диссоциируют: Cs2SO4 à 2 Cs++SO42 - | 2) Соль, образованная сильным основанием и слабой кислотой - гидролиз ПО АНИОНУ . Анион слабой кислоты отрывает от воды ионы водорода , связывает их. В растворе образуется избыток ионов ОН - - среда щелочная. ПРИМЕР: Гидролизу по аниону подвергаются соли - Na2S, KF, K3PO4 , Na2CO3, Cs2SO3, KCN, KClO, и кислые соли этих кислот. K 3 PO 4 – соль, образованная слабой кислотой и сильным основанием. Гидролизуется фосфат-анион. PO 4 3- + НОН ⇄ НРО42-+ОН- K 3 PO 4 + Н2О ⇄ К2НРО4 + КОН (это первая ступень гидролиза, остальные 2 идут в очень малой степени) |
3) Соль, образованная слабым основанием и сильной кислотой - гидролиз ПО КАТИОНУ . Катион слабого основания отрывает от воды ион ОН-, связывает его. В растворе остаётся избыток ионов H+ - среда кислая. ПРИМЕР: Гидролизу по катиону подвергаются соли - CuCl2, NH4Cl, Al(NO3)3, Cr2(SO4)3 . Cu SO 4 – соль, образованная слабым основанием и сильной кислотой. Гидролизуется катион меди: Cu +2 + НОН ⇄ CuOH + + H + 2 CuSO 4 +2 H 2 O ⇄ (CuOH )2 SO 4 + H 2 SO 4 | 4) Соль, образованная слабым основанием и слабой кислотой - гидролиз И ПО КАТИОНУ И ПО АНИОНУ. Если какие-либо из продуктов выделяются в виде осадка или газа, то гидролиз необратимый , если оба продукта гидролиза остаются в растворе - гидролиз обратимый. ПРИМЕР: Гидролизуются соли – · Al2S3,Cr2S3(необратимо): Al2S3 + H2O à Al(OH)3 ¯ + H2S · NH4F, CH3COONH4(обратимо) NH4F + H 2 O ⇄ NH4OH + HF |
Взаимный гидролиз двух солей.
Он происходит при попытке получить с помощью обменной реакции солей, которые в водном растворе полностью гидролизованы. При этом происходит взаимный гидролиз – т. е. катион металла связывает ОН-группы, а анион кислоты – Н+
1) Соли металлов со степенью окисления +3 и соли летучих кислот (карбонаты, сульфиды, сульфиты) – при их взаимном гидролизе образуется осадок гидроксида и газ:
2AlCl3 + 3K2S + 6H2O à 2Al(OH)3¯ + 3H2S + 6KCl
(Fe3+, Cr3+) (SO32-, CO32-) (SO2, CO2)
2) Соли металлов со степенью окисления +2 (кроме кальция, стронция и бария) и растворимые карбонаты также вместе гидролизуются, но при этом образуется осадок ОСНОВНОГО КАРБОНАТА металла:
2 CuCl2 + 2Na2CO3 + H2O à (CuOH)2CO3 + CO2 + 4 NaCl
(все 2+, кроме Са, Sr, Ba)
Характеристика процесса гидролиза:
1) Процесс гидролиза является обратимым , протекает не до конца, а только до момента РАВНОВЕСИЯ;
2) Процесс гидролиза – обратный для реакции НЕЙТРАЛИЗАЦИИ, следовательно, гидролиз - эндотермический процесс (протекает с поглощением теплоты).
KF + H2O ⇄ HF + KOH – Q
Какие факторы усиливают гидролиз?
1. Нагревание – при увеличении температуры равновесие смещается в сторону ЭНДОТЕРМИЧЕСКОЙ реакции – гидролиз усиливается;
2. Добавление воды – т. к. вода является исходным веществом в реакции гидролиза, то разбавление раствора усиливает гидролиз.
Как подавить (ослабить) процесс гидролиза?
Часто необходимо не допустить гидролиза. Для этого:
1. Раствор делают максимально концентрированным (уменьшают количество воды);
2. Для смещения равновесия влево добавляют один из продуктов гидролиза – кислоту , если идёт гидролиз по катиону или щёлочь, если идёт гидролиз по аниону.
Пример: как подавить гидролиз хлорида алюминия ?
Хлорид алюминия AlCl 3 – это соль, образованная слабым основанием и сильной кислотой – гидролизуется по катиону:
Al +3 + HOH ⇄ AlOH +2 + H +
Среда – кислая. Следовательно, для подавления гидролиза необходимо добавить еще кислоты. Кроме того, следует сделать раствор наиболее концентрированным.
 HCO3 + OH
HCO3 + OH